УДК 347.028:547-3
Колотілова Ю.Ю.
Кандидат хімічних наук
Начальник сектору дослідження патентно-інформаційних баз даних
Державного підприємства "Український інститут
промислової власності"
ДЕЯКІ ПРАВОВІ КОЛІЗІЇ, ЩО ВИНИКАЮТЬ ПІД ЧАС
ВИКОРИСТАННЯ ФОРМУЛИ ТИПУ "ПРОДУКТ ЧЕРЕЗ СПОСІБ"
У статті розглянуто особливості формул типу "продукт через спосіб" та проаналізовано можливі правові наслідки, до яких може призвести надання правового захисту хімічним сполукам, заявленим через спосіб їх одержання.
Ключові слова: продукт через спосіб, правовий, групи хімічних сполук, продовження строку дії патенту, лікарський засіб.
В статье рассмотрены особенности формул типа "продукт через способ" и проанализированы возможные правовые последствия, к которым может привести предоставление правовой защиты химическим соединениям, заявленным через способ их получения.
Ключевые слова: продукт через способ, правовой, группы химических соединений, продление срока действия патента, лекарственное средство.
The article discloses peculiarities of product-by-process claims and analyses possible legal consequences of legal protection for chemical compounds claimed by process for preparation thereof.
Keywords: product-by-process, legal, groups of chemical compounds, prolongation of patent term, drug.
Актуальність надання патентного захисту таким об’єктам, як органічні сполуки, пов’язана з реєстрацією лікарських засобів, захистом прав виробників оригінальних препаратів і патентуванням генериків.
Одна з проблем, що виникає як під час розгляду заявок на сполуки, так і в процесі розгляду клопотань щодо продовження строку дії патентів на сполуки – активні компоненти лікарських засобів, – випливає із законодавчо встановленої можливості поширення правового захисту на продукт, одержаний конкретним способом, якщо об’єктом винаходу є саме цей спосіб.
Деякі правові колізії виникають пі час розгляду справ, що стосуються відповідності діючої речовини лікарського засобу (а саме, сполуки), якій надається правова охорона як продукту, та цієї самої речовини під час реєстрації лікарського засобу, зокрема, у разі вимоги продовження дії патенту на винахід у зв’язку із зареєстрованим лікарським засобом.
В основному виникнення цих колізій пов’язане з трактуванням та правовими наслідками так званої формули типу "продукт через спосіб", що регламентується частиною шостою статті 6 Закону України "Про охорону прав на винаходи та корисні моделі" [1] (далі – Закон), викладеною таким чином: дія патенту (деклараційного патенту), виданого на спосіб одержання продукту, поширюється й на продукт, безпосередньо одержаний цим способом.
Перше питання у зв’язку з цим випливає вже із самої редакції такого формулювання: у Цивільному кодексі України [2] немає поняття "дія патенту", а є лише "правова охорона". Таким чином, уже перша частина вищенаведеного речення потребує коригування відповідно до положення про верховенство права.
Щодо другої частини формулювання, то перед тим, як розпочати її аналіз, варто навести ще деякі статті Закону, а саме: згідно з частиною четвертою статті 6 Закону строк дії патенту на винахід, об’єктом якого є лікарський засіб, засіб захисту тварин, засіб захисту рослин тощо, використання якого потребує дозволу відповідного компетентного органу, може бути продовжено за клопотанням власника цього патенту на строк, що дорівнює періоду між датою подання заявки та датою одержання такого дозволу, але не більше ніж на п’ять років. За подання клопотання сплачується збір.
Відповідно до статті 28 Закону використанням винаходу (корисної моделі) визнається:
- виготовлення продукту із застосуванням запатентованого винаходу (корисної моделі), застосування такого продукту, пропонування для продажу, у тому числі через Інтернет, продаж, імпорт (ввезення) та інше введення його в цивільний оборот або зберігання такого продукту в зазначених цілях;
- застосування процесу, що охороняється патентом, або пропонування його для застосування в Україні, якщо особа, яка пропонує цей процес, знає про те, що його застосування забороняється без згоди власника патенту або, виходячи з обставин, це й так є очевидним.
Продукт визнається виготовленим із застосуванням запатентованого винаходу (корисної моделі), якщо при цьому використано кожну ознаку, включену до незалежного пункту формули винаходу (корисної моделі), або ознаку, еквівалентну їй.
Процес, що охороняється патентом, визнається застосованим, якщо використано кожну ознаку, включену до незалежного пункту формули винаходу, або ознаку, еквівалентну їй.
Будь-який продукт, процес виготовлення якого охороняється патентом, якщо немає доказів протилежного, вважається виготовленим із застосуванням цього процесу за умови виконання принаймні однієї з двох вимог:
- продукт, виготовлений із застосуванням процесу, що охороняється патентом, є новим;
- є підстави вважати, що зазначений продукт виготовлено із застосуванням цього процесу й власник патенту не в змозі шляхом прийнятних зусиль визначити процес, який застосовувався під час виготовлення цього продукту.
У такому разі обов’язок доведення того, що процес виготовлення продукту, ідентичного тому, що виготовляється із застосуванням процесу, який охороняється патентом, відрізняється від останнього, покладається на особу, щодо якої є достатні підстави вважати, що вона порушує права власника патенту.
Тепер, коли ми ознайомилися з тим, яким чином національне законодавство регламентує надання правової охорони продукту через спосіб його одержання та як визначає використання винаходу, доцільно буде розглянути на конкретному прикладі правові колізії, до виникнення яких може призвести таке формулювання частини шостої статті 6 Закону, особливо у випадках звернень щодо продовження дії патенту під час реєстрації лікарського засобу.
Як відомо, у Законі України "Про лікарські засоби" [3] зазначено, що для державної реєстрації лікарських засобів, які базуються на об’єктах інтелектуальної власності або мають відношення до них, яко на ці об’єкти відповідно до законів України видано патент, заявник подає копію патенту або ліцензії, згідно з якою дозволяється виробництво та продаж зареєстрованого лікарського засобу. Заявники подають лист, у якому вказується, що права третьої сторони, захищені патентом, не порушуються у зв’язку з реєстрацією лікарського засобу.
На зареєстрований лікарський засіб заявнику видається посвідчення, у якому зазначається строк дії, протягом якого лікарський засіб дозволяється застосувувати в Україні. Лікарський засіб може застосовуватися в Україні протягом п’яти років з дня його державної реєстрації. За бажанням особи, яка подала заяву про державну реєстрацію лікарського засобу, строк, протягом якого дозволяється його застосування на території України, за рішенням реєстраційного органу може бути скорочено.
Таким чином, згідно з Наказом "Про порядок продовження строку дії патенту на винахід, об’єктом якого є засіб, використання якого потребує дозволу компетентного органу" [4] у власника патенту є право вимагати продовження строку дії патенту на винахід на п’ять років, якщо він одночасно є й власником зареєстрованого лікарського засобу.
Якщо об’єктом винаходу є сам продукт, тобто його захищено як такий, суперечок не виникає. Проблеми з’являються в разі, коли захищено спосіб одержання продукту, тобто у випадку так званої формули "продукт через спосіб".
Особливо це стосується ситуацій, коли захищено спосіб одержання не однієї конкретної сполуки (продукту), а групи сполук, що підпадають під одну й ту саму структурну формулу. У такому випадку застосування вищезазначеної норми закону призводить до дуже широкої охорони, оскільки продуктом є невизначена кількість сполук, які мають однакову загальну структурну формулу (формулу Маркуша).
Як приклад розглянемо ситуацію з патентом України на винахід № 2668.
До Державного департаменту інтелектуальної власності (далі – Держдепартамент) надійшло звернення щодо продовження строку дії вищезазначеного патенту на п’ять років у зв’язку з тим, що "заявником __________було отримано перше Реєстраційне посвідчення на лікарський засіб № 2882 від 25.02.1998, що надає МОЗ України лише у 1998 р.
Заявник продовжує реєструвати цей препарат у відповідних органах на протягом десяти років і підтвердження цьому є реєстраційні посвідчення №Р. 12.99/01251 від 23.12.1999 та №П.03.03/06141 від 14.03.2003 (додаються) що надає МОЗ України Державний фармакологічний центр".
Вищезгаданий патент являє собою перереєстрований патент Радянського Союзу 4356404/SU, виданий на спосіб одержання групи органічних сполук, що підпадають під одну загальну структурну формулу, та має назву "СПОСІБ ОТРИМАННЯ ПОХІДНИХ ГУАНІНУ АБО IX КИСЛОТНО-АДИТИВНИХ ФАРМАЦЕВТИЧНО ПРИЙНЯТИХ СОЛЕЙ". Цей охоронний документ виданий компанії Дзе Веллкам Фаундейшн (дата подання заявки – 12.08.1988, дата видачі патенту – 26.12.1994, опубліковано в Бюлетені № 5 – 1).
Формула винаходу, що регламентує обсяг правової охорони, складається з одного незалежного пункту, який уточнюється одним залежним, а саме:
- "Способ получения производных гуанина общей формулы І
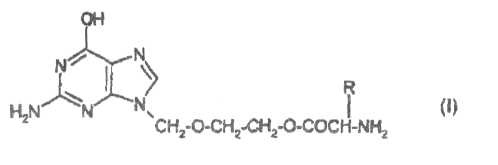 где R – группа – СН(СН3)2 или группа –СН(СН3 СН2СН3, или их кислотно аддитивных фармацевтически приемлемых солей, отличающийся тем, что 9 (гидроксиэтоксиметил)гуанин подвергают взаимодействию с N-защищенным валином или изолейцином в присутствии дициклогексилкарбодиимида и, возможно, основания в органическим растворителе с последующим удалением защитной группы и выделением целевого продукта в виде основания или переведением его в соль действием кислоты.
где R – группа – СН(СН3)2 или группа –СН(СН3 СН2СН3, или их кислотно аддитивных фармацевтически приемлемых солей, отличающийся тем, что 9 (гидроксиэтоксиметил)гуанин подвергают взаимодействию с N-защищенным валином или изолейцином в присутствии дициклогексилкарбодиимида и, возможно, основания в органическим растворителе с последующим удалением защитной группы и выделением целевого продукта в виде основания или переведением его в соль действием кислоты. - Способ по п. 1, отличающийся тем, что в качестве кислоты используют соляную кислоту".
Експертизою в лютому 2008 року у відповідь на поставлене перед нею запитання, чи є діюча речовина лікарського засобу "Вальтрекс" – валацикловіру гідрохлорид – об’єктом винаходу за патентом України на винахід № 2668, була надана така відповідь: об’єктом вищезазначеного патенту є спосіб одержання похідних гуаніну або їх кислотно-адитивних фармацевтично прийнятних солей, а не самі похідні гуаніну або їх кислотно-адитивні фармацевтично прийнятні солі. Діюча речовина лікарського засобу "ВАЛЬТРЕКС" – валацикловіру гідро хлорид – не є об’єктом винаходу за патентом України на винахід № 2668. На підставі цієї відповіді Держдепартаментом у березні 2008 року було прийняте рішення про відмову в продовженні строку дії патенту на винахід № 2668 відповідно до Наказу [4].
Але заявник не погодився з таким рішенням, і в липні 2008 року до Держдепартаменту надійшло клопотання щодо продовження строку дії вищезазначеного патенту на п’ять років. Зокрема, у тексті клопотання зазначалося:
"Заявник не згоден з Рішенням Держдепартаменту від 05.03.2008 і просимо переглянути питання щодо правомірності відмови в продовженні строку дії Патенту № 2668 "СПОСІБ ОТРИМАННЯ ПОХІДНИХ ГУАНІНУ АБО IХ КИСЛОТНО-АДИТИВНИХ ФАРМАЦЕВТИЧНО ПРИЙНЯТИХ СОЛЕЙ" (див. Додаток 2) на додаткові 5 років у зв’язку з наведеними нижче доводами, які свідчать про не дотриманості процедури розгляду продовження строку дії патенту на винахід та про помилковість зазначеного Рішення.
У частині четвертій статті 6 Закону зазначається:
"Строк дії патенту на винахід, об’єктом якого є лікарський засіб, засіб захисту тварин, засіб захисту рослин тощо, використання якого потребує дозволу відповідного компетентного органу, може бути продовжено за клопотанням власника цього патенту на строк, що дорівнює періоду між датою подання заявки та датою одержання такого дозволу, але не більше ніж на 5 років. За подання клопотання сплачується збір". Заявник вчасно – 11 лютого 2008 року – сплатив збір і разом з клопотанням про продовження строку дії патенту на максимально дозволений законом – п’ять років – подав відповідні документи до Держдепартаменту на підставі того, що заявка № 4356404/SU, за якою одержано патент України № 2668, була подана 12.08.1988, а перше реєстраційне посвідчення № 2882 на лікарський засіб "Вальтрекс" було одержане апелянтом лише 25.02.1998.
Згідно з розділом 3 пункту 3.5 Наказу Міністерства охорони здоров’я України від 26.08.2005 № 426 "Про Порядок проведення експертизи матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також експертизи матеріалів про внесення змін до реєстраційних матеріалів протягом дії реєстраційного посвідчення" [4] (далі – Наказ), на який посилається виконавець Держдепартаменту, встановлено, що в разі невідповідності клопотання вимогам, зазначеним у розділах 1 і 2, або в разі виникнення обґрунтованих сумнівів щодо вірогідності інформації, яку містять подані документи, Держдепартамент направляє власнику патенту повідомлення із зазначенням невідповідностей та/або запитом про надання додаткових документів, необхідних для приймання рішення.
Згідно з пунктом 3.6 того самого Наказу власнику патенту надається два місяці від дати одержання ним повідомлення або запиту Держдепартаменту для усунення невідповідностей та/або надання додаткових документів. Якщо власник у встановлений строк надасть відповідь та/або додаткові документи, то Держдепартамент розглядає їх протягом місяця від дати надходження.
Згідно з вищевикладеним рішення від 5 березня 2008 року було винесене передчасно, тим самим позбавивши власника патенту права надати необхідні документи чи обґрунтовані докази на користь задоволення відповідного клопотання, а отже, було порушено процедуру розгляду продовження строку дії патенту на винахід, об’єктом якого є засіб, використання якого потребує дозволу компетентного органу.
Додатково Заявник наголошує: припущення, що діюча речовина лікарського засобу "Вальтрекс" – валацикловіру гідрохлорид – не є об’єктом винаходу за патентом України на винахід № 2668 "СПОСІБ ОТРИМАННЯ ПОХІДНИХ ГУАНІНУ АБО ЇХ КИСЛОТНО-АДИТИВНИХ ФАРМАЦЕВТИЧНО ПРИЙНЯТИХ СОЛЕЙ", як зазначено в супроводжувальному листі (від 06.03.08 № 16-11/1344) до рішення, є хибним з огляду на таке:
Забезпечення прямого захисту біологічно активної речовини – активного інгредієнта нового лікарського засобу – є найефективнішим способом досягнення монопольних позицій на ринку та захисту прав винахідника.
Патент України є перереєстрацією патенту Радянського Союзу SU 1634138 A3 і сформульований як такий, що прямо вказує на спосіб одержання продукту, оскільки тільки з прийняттям закону України виникла правова основа для прямого захисту патентом хімічних речовин та лікарських засобів, що було неможливо за умов раніше чинного Положення про відкриття, винаходи та раціоналістичні пропозиції. Відтак, для збереження прав власника патенту чинним законодавством передбачено, що: "Дія патенту (деклараційного патенту), виданого на спосіб одержання продукту, поширюється і на продукт, безпосередньо одержаний цим способом" (див. частину шосту статті 6 Закону).
Формула винаходу патенту № 2668 охоплює переважний спосіб одержання діючої речовини лікарського засобу "Вальтрекс".
Вальтрекс – валацикловір (L-валіновий ефір 9-[(2- оксіетокси)метил]гуанін) – є орально активним L-валіновим складним ефіром ацикловіру та має таку хімічну структуру:
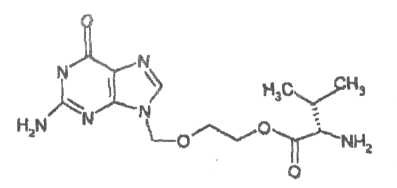
Він продається у формі хлористоводневої солі (солі гідрохлориду).
У патенті України № 2668 заявлено спосіб одержання сполук загальної формули І (див. рис. 1) або їх фармацевтично прийнятних кислотно-адитивних солей.
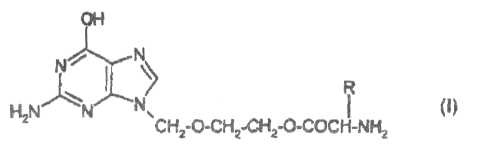
Рисунок 1.
R позначає -СН(СН3)2 або -СН(СН3)СН2СН3, шляхом введення в реакцію ацикловіру з N-захищеним валіном або ізолейцином і виділення продукту у вигляді основи або переведення його в сіль дією кислоти, згідно з пунктом 2
формули це є соляна (хлористоводнева) кислота (НСl).
Очевидно, що, коли R позначає -СН(СН3)2, то сполука формули (І) є валацикловіром.
У пункті 2 формули патенту України вказано, що, коли утворюється сіль, переважно це є сіль гідрохлориду [з використанням соляної (хлористоводневої) кислоти].
Отже, у патенті чітко розкритий спосіб одержання лікарського засобу "Вальтрекс", активним інгредієнтом якого є валацикловіру гідрохлорид.
На підтвердження цього разом з клопотанням від 11 березня 2008 року заявник надав "Схему процесу синтезу валацикловіру гідрохлорид", який є діючою речовиною лікарського засобу "Вальтрекс".
Заявник також звертає увагу, що виведення препарату на фармацевтичний ринок супроводжується процедурою його патентування – захистом хімічної формули, нового штаму мікроорганізму, способу одержання тощо.
Обсяг прав, надаваних патентом, визначається формулою винаходу.
Формула винаходу на нову хімічну сполуку включає тільки її структурну формулу (чи загальну структурну формулу для групи сполук) або її назву (або й те, й інше).
Водночас згідно з чинним законодавством та практикою використання лікарського засобу потребує дозволу відповідного компетентного органу, одержання якого, як правило, забирає певний час. А отже, для збереження та захисту прав заявника в повній мірі забезпечено можливість додаткового продовження строку чинності патенту на строк, що дорівнює періоду між датою подання заявки та датою одержання такого дозволу, але не більше ніж на п’ять років (див. Закон, частину четверту статті 6 абзацу п’ятого).
Патент України на винахід № 2668 охоплює продукт через спосіб, використовуваний для виробництва, та, на переконання заявника, може бути продовжений як такий. Заявник не розуміє причину виникнення припущення, що валацикловір НСl не охоплюється цим патентом.
На підставі вищевикладених обставин і доказів заявник вважає, що експертизою не було враховано всіх даних цієї справи та положень Закону й Наказу [4].
З наведеного вище цитування очевидно, що заявник апелює до норми Закону, встановленої частною шостою статті 6, та наполягає, що правова охорона поширюється на вальцикловір як на хімічну сполуку, що підпадає під загальну структурну формулу (І), спосіб одержання якої заявляється.
Але ж у статті 28 Закону зазначається, що використані можуть бути лише ознаки способу, тоді як про жодну ознаку продукту, окрім загальної родової структурної формули, не йдеться.
Постає питання: яким саме чином можна говорити про використання продукту (тобто__________, групи сполук) у трактуванні статті 28 Закону, якщо продукт визнається виготовленим із застосуванням запатентованого винаходу (корисної моделі), якщо при цьому використано кожну ознаку, включену до незалежного пункту формули винаходу (корисної моделі), або ознаку, еквівалентну їй.
У випадку реєстрації лікарського засобу, активною складовою якого є продукт, одержаний запатентованим способом, будуть порушені права інших власників патентів на винаходи, об’єктом яких є інший спосіб або цей самий продукт, але одержаний іншим способом, що спричинить ще низку правових питань.
Крім того, у цьому випадку будуть порушені права третіх осіб, які вимагатимуть надання правового захисту будь-якому продукту, що підпадатиме під вищевказану родову структурну формулу.
Таким чином, якщо аналізувати тільки формулу винаходу за патентом України № 2668, можна дійти цілком обґрунтованого висновку, що, оскільки об’єктом винаходу відповідно до формули винаходу є спосіб, а жодних ознак продукту (тобто, вальцикловіру), не наведено, то заявнику має бути відмовлено в продовженні строку дії патенту на винахід, оскільки зареєстрованим у відповідних органах є продукт, не захищений патентом України на винахід.
Остаточно проаналізувавши доводи заявника, експертиза запропонувала таке: якщо в описі до патенту України № 2668 містяться відомості, у яких наведено ознаки самого продукту, одержаного заявленим способом (а саме, в прикладах реалізації способу за заявленим винаходом), і якщо доведено, що продукт, одержаний цим способом, є продуктом, заявленим для реєстрації в державних органах реєстрації лікарських засобів, то може бути визнано, що продукт захищено, і дію патенту може бути подовжено.
У цьому конкретному випадку питання з правової точки зору перейшло в площину хімії, оскільки в описі до патенту наведено ознаки та доведено одержання вальцикловіру гідрохлориду моногідрату, а в реєстраційному посвідченні вказаний вальцикловір гідрохлорид. Оскільки незрозуміло, чи є ці форми по суті однаковими, як саме впливає наявність аквагрупи на властивості діючої речовини, заявник має довести тотожність хімічної сполуки, описаної в прикладах, та лікарського засобу, що був зареєстрований як такий. Але в разі, якщо такі відомості надані не будуть, то в клопотанні щодо продовження строку дії патенту України на винахід у зв’язку з реєстрацією лікарського засобу буде відмовлено.
Узагальнюючи викладене вище, можна дійти висновку, що правовий захист формули "продукт через спосіб" на цей час є недосконалим. Під час надання правової охорони хімічним сполукам, особливо групам хімічних сполук, переважно таким, що підпадають під загальну родову структурну формулу (формулу Маркуша), заявленим формулою "продукт через спосіб", заявники та експерти стикаються з низкою проблем, а саме:
- недостатність розкриття;
- висока імовірність відмови, якщо є подібні продукти або способи;
- значні обмеження в способі для доведення того, що заявлений продукт одержано тільки таким способом;
- продукт виявиться незахищеним, якщо він одержаний іншим способом.
Список літератури
- Закон України "Про охорону прав на винаходи і корисні моделі" / У редакції Закону від 01.06.2000 № 1771-ІІІ, із змінами, внесеними згідно із Законом від 21.12.2000 №2188-ІІІ, та із змінами, внесеними згідно із Законом від 10.01.2002 № 2921-III, Відомості Верховної Ради, 2002, № 16, ст.114, зі змінами і доповненнями від 22.05.2003.
- Цивільний кодекс України
- Закон України "Про лікарські засоби" (Відомості Верховної Ради, 1996, № 22, ст. 86 із змінами і доповненнями, внесеними Законом України від 19.01.2006 № 3370-IV (3370-15 ).
- Наказ Міністерства охорони здоров’я України від 26.08.2005 № 426 "Про Порядок проведення експертизи матеріалів на лікарські засоби, що подаються на державну реєстрацію (перереєстрацію), а також експертизи матеріалів про внесення змін до реєстраційних матеріалів протягом дії реєстраційного посвідчення" та Наказ від 01.03.2006 № 95 "Про внесення змін і доповнень до наказу МОЗ України від 26.08.2005 № 426".
